PD-1之后,CDE鼓励开发另一种单抗
国产EGFR单抗的研发步伐会轻快不少
PD-1之后,EGFR靶点的春天来了。
9月8日,国家药监局药审中心(CDE)官网公布《西妥昔单抗注射液生物类似药临床试验设计指导原则(征求意见稿)》,旨在推动国内企业研发西妥昔单抗生物类似药的进度。

图源:国家药品监督管理局药品审评中心
CDE并不常发布类似针对单品的“指导原则”。健识局粗略统计,2019年以来CDE仅明确鼓励过三款生物类似药的研发:治疗肥胖用的利拉鲁肽、治疗骨质疏松的地舒单抗,以及这次的西妥昔单抗。
西妥昔单抗是一种EGFR靶点的lgG1亚型的人鼠嵌合型单抗,原研药是礼来开发的,2007年在中国由默克负责上市销售,目前获批两项适应症:结直肠癌和头颈部鳞癌。
CDE的推动往往会掀起行业研发热潮。2018年2月,CDE曾公布《抗PD-1/PD -L1单抗品种申报上市的资料数据基本要求》,加快PD-1类药物的上市进程。3年后的今天,国内已经有6款PD-1上市,已经成为红海。
这一次CDE打开了新的蓝海大门:EGFR单抗。
01 小分子发展迅猛,单抗几乎停滞
目前,国内市场上主要有两类EGFR靶点产品:小分子的EGFR抑制剂(EGFR-TKI)和EGFR单抗。开发小分子EGFR抑制剂的企业远多于EGFR单抗,更迭速度也更快。
小分子EGFR抑制剂的市场份额远高于EGFR单抗,这是因为在治疗非小细胞肺癌时,EGFR小分子药物更有优势。广为人知的抗肺癌神药“易瑞沙”,就是典型的小分子EGFR药物。
肺癌是中国发病率最高的癌种,其中非小细胞肺癌占比达85%。2014年-2018年,中国非小细胞肺癌年新增病例从64.7万人增长至73.7万人。2023年,预计年新增病例将达85.9万人。
相对来说,小分子的EGFR抑制剂开发起来更容易,患者用药方便,依从性也好,因此受药企偏爱。如今,国内获批上市的EGFR抑制剂已从一代发展到三代,第四代也正在研发中。

即便已有品种上市,还是有不少企业在第三代小分子EGFR抑制剂的研发道路上狂奔,包括奥赛康、南京圣和药业、苏州润新生物等。目前,第三代小分子EGFR抑制剂中,阿斯利康的奥希替尼和豪森药业的阿美替尼已进入医保。
相对来说,大分子的EGFR单抗鲜有企业研发。EGFR单抗是生物药,研发经费和时间投入要比小分子药物多得多;同时,生物药的治疗需要医生严格操作,依从性不好。
更为关键的是,EGFR单抗目前来看对于头颈癌、KRAS野生型结直肠癌的疗效显著。但这两种肿瘤都不算大癌种,市场想象空间不大,自然也就没有企业原因投入精力。
02 EGFR单抗的新机遇
就当下的国内市场而言,EGFR单抗的未来并不惨淡。
据Frost & Sullivan 报告,2014年到2018年,我国头颈癌患年新增病例从12.5万人增长至13.7万例,2023年预计会增至15.2万人;而结直肠癌患病人数,从2018年到2023年,预计年新增病例将由42.4万上升至48.9万,其中,KRAS野生型占比为53%到65%。平均下来,中国每年都会新增超过25万例适用EGFR单抗的患者。
两个小癌种每年适用EGFR单抗的患者总数将超过40万,同时EGFR在多种实体瘤存在突变现象,具备广谱靶点的特质。东方财富证券就曾发布过研究报告称,EGFR在多种癌种中均出现高表达,肺癌中高表达比例为30%到80%,食管癌中比例为43%到89%。
目前全球上市的EGFR单抗有四款。其中两款已经入中国市场,分别是西妥昔单抗和尼妥珠单抗,市场竞争力度较小。如果未来EGFR单抗开发出更大的适应症,必然将成为重磅单品。
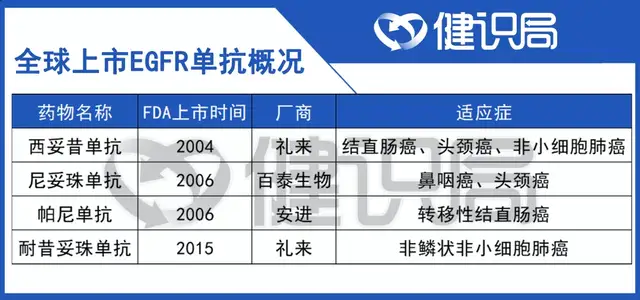
图源:国信证券研究所 & 公开资料
这样看来,EGFR单抗可能会迎来春天,CDE发文鼓励,也算是未雨绸缪。
据不完全统计,当前国内至少有9家企业正在开发EGFR单抗。其中,科伦制药、齐鲁制药、佛山安泽普生物进度最快,已处于Ⅲ期临床;神州细胞、三生国建、复宏汉霖则守在第二梯队。

图源:CDE官网 & 公司公告
参照此前药监局对PD-1的扶持效果,EGFR靶点有望在政策扶助下,成为一块新兴热门领域。至于谁能在CDE关爱下抢先“撞线”上市,相信不久就会有答案。
文丨烟酰胺
设计丨莫羽汐
运营丨薄荷
每天两篇深度稿件,解码医药健康
TOP STORIES
相 关 推 荐




 京公网安备11010502039624号
京公网安备11010502039624号