一致性评价、带量采购步步紧逼,大批王牌药市场难保!
通过一致性评价仿制药临床替代来了。
下周四(12月6日)“4+7”带量采购试点即将开标,这个关键时刻(11月29日)乐普医疗发布公告,旗下硫酸氢氯吡格雷片(75mg、25mg)通过了一致性评价。

硫酸氢氯吡格雷片在医保局带量采购范围内,且两规格采购量分别达到18320.56万片(25mg)和5746.59万片(75mg)。行业预估总金额可以达到8亿元。
硫酸氢氯吡格雷片主要用于心血管领域,目前国内主要有3家企业的产品——原研药赛诺菲的波立维,首批通过一致性评价的信立泰泰嘉和刚刚通过一致性评价的乐普医疗的帅泰(25mg)、帅信(75mg)。
多年来,虽然波立维早已过专利期,在美国销量快速下滑,遭遇“专利悬崖”,但仍占据我国市场主导地位。
2017年,氯吡格雷是市场最大的品种,国内销售额超过110亿元,艾美达数据显示,2017年前三季度全国样本公立医院氯吡格雷的采购总额中,波立维的占比还达到58.99%;深圳信立泰的泰嘉,市场占比为30.16%。
自2017年底,信立泰的泰嘉(硫酸氢氯吡格雷片)作为首批通过一致性评价品种承接各项利好以来,波立维在国内的增长速度已经放缓。
中国医药工业信息中心医院处方分析系统RAS数据显示,今年泰嘉的市场占有率达到46%,首次超过波立维的45.2%;乐普的帅泰(25mg)和帅信(75mg)分别占3.1%和5.7%。
结合带量采购,用试点城市60%到70%的市场,换取相关药品的最低价的逻辑,以及各地药采联动全国最低价的规则,可以看出,占有较大市场份额的波立维、泰嘉处境非常不利,毕竟降价过低,会影响更大市场。反而对市场份额较小的帅泰、帅信是重大利好。
而回到通过一致性评价仿制药临床替代原研药的属性,随着通过一致性评价仿制药品种的不断增加,跨国药企在中国忍痛割舍已过专利期多年的“王牌”品种的日子不远了。

121仿制药过一致性评价
原研药面临大规模临床替代
一致性评价进程正在加快。
据业界统计,仅11月份就有12个药品通过一致性评价,包括
乐普医疗的硫酸氢氯吡格雷片(75mg、25mg)
东瑞制药的恩替卡韦分散片(0.5mg)、苯磺酸氨氯地平片(5mg)
江苏德源的盐酸二甲双胍缓释片(0.5g)
华东医药的阿卡波糖片(50mg)
石药集团的阿莫西林胶囊(0.5g、0.25g)
南京正大天晴的恩替卡韦胶囊(0.5mg)
四川海思科的恩替卡韦胶囊(0.5mg)
重庆药友的盐酸克林霉素胶囊(75mg、150mg)
广东华南的盐酸二甲双胍片(0.25g)
一举增加两个通过一致评价品种企业达到3家以上的品种。
11月23日,国家食药监管总局药品审评中心(CDE)公布一致性评价最新进展称,截至2018年10月19日,已受理一致性评价申请447件(177个品种),已完成一致性评价药品127个品种。(详见>>CDE:一致性评价淘汰升级,超4000品种大洗牌!)
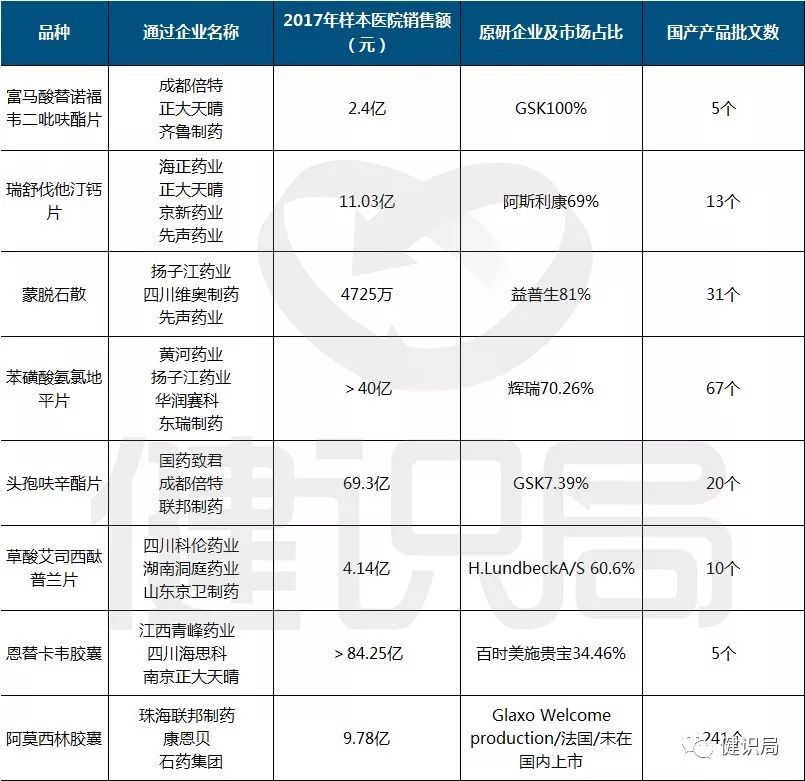
健识君根据公开数据整理出已通过或视同通过一致性评价的121个仿制药产品,根据国办4月份发布的《关于改革完善仿制药供应保障及使用政策的意见》,它们在医生处方、集中采购、医保支付方面与原研药平权,将临床替代原研药,以促进药价回归合理,减缓医疗费用增速。
从中可以看到,对应的原研药中,涉及众多知名跨国药企的”王牌“品种,如:赛诺菲的波立维、安博维、安博诺,阿斯利康的易瑞沙、可定;辉瑞的活络喜、立普妥;施贵宝的博路定;拜耳的拜糖平;等等。
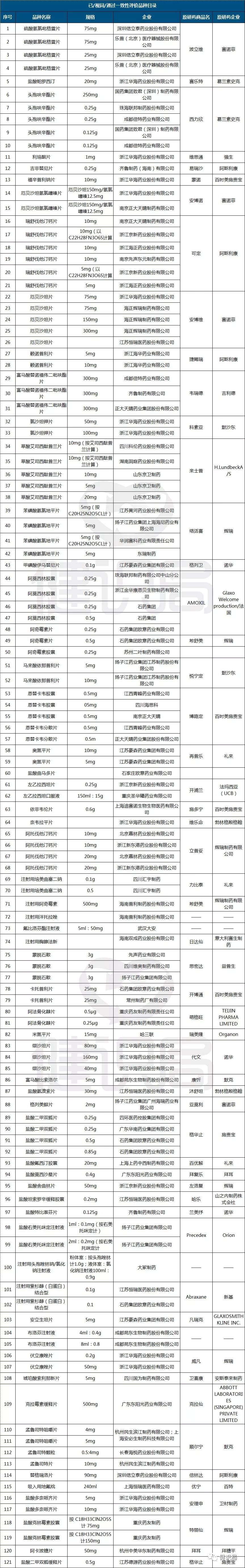
分析人士指出,未来,在通过一致性评价药品的竞争下,这些已过专利期,但在我国没有立即迎来“专利悬崖”的“王牌药”,将面临大规模的临床替代。
带量采购撬动
大批“王牌”药将失去中国市场
事实上,很多“王牌”药的专利已经过期多年,在全球市场上,都遇到了发展瓶颈、“专利悬崖”,但在中国,发展势头仍然强劲。
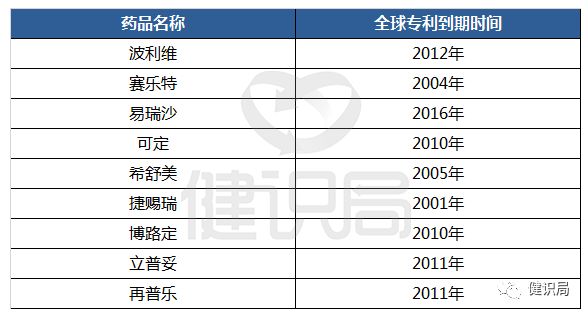
如2011年专利已经到期的立普妥,2016年在国内公立医院终端销售额达到60.86亿元,占据69.26%的市场份额,而排在第二位的国产品牌北京嘉林的“阿乐”仅占据27.74%。
这与我国仿制药疗效、质量难以与原研药抗衡有关,而在大批仿制药努力提高质量的同时,药品集中采购政策制定及落实,也是重要的撬动杠杆。
或许2017年底,首批通过一致性评价仿制药名单公示之时,业界还有观望和怀疑,经过2018年,通过一致性评价仿制药利好政策在各地相继落地后,过专利期原研被替代的趋势已经基本确定。
特别是今年9月份以来,国家医保局组织的“4+7”城市试点带量采购方案,提出以60%-70%市场换取最低价。在这场竞价比拼中,原研药、通过一致性评价仿制药、未通过一致性评价仿制药,将在一个平台上竞争。
而上海市近日发布的带量采购实施细则中,更是明确,“符合本次集中采购申报要求的同品种未中选的最高价药品,必须在本市2017年中标价(或挂网价)基础上,根据价差实现梯度降价后(以中选价托底)方可继续采购使用,价差较大的须进一步加大降价幅度”。
这意味着,在带量采购中,原研药无论是否中标,要想继续在当地市场销售,就必须降价,否则就退出市场。
一位业内人士曾向健识局表示,如果仿制药可以代替原研药,那么原研药也就没有存在的必要。也就是说,随着我国仿制药质量的不断提高,跨国药企将不得不接受旗下“王牌药”痛失中国市场的事实。
TOP STORIES
相 关 推 荐




 京公网安备11010502039624号
京公网安备11010502039624号